Bagaimana peranan katalis dalam mempercepat laju reaksi? Pertanyaan ini menjadi kunci pemahaman proses kimiawi di berbagai skala, dari reaksi sederhana di dapur hingga proses industri berskala besar. Katalis, zat ajaib yang mampu meningkatkan kecepatan reaksi tanpa ikut bereaksi secara permanen, merupakan pilar penting dalam berbagai inovasi teknologi. Bayangkan saja, tanpa katalis, produksi pupuk, plastik, dan bahkan bensin akan jauh lebih lambat dan mahal. Penggunaan katalis yang tepat memungkinkan reaksi berlangsung lebih efisien, menghasilkan produk yang lebih banyak dengan energi yang lebih sedikit, sebuah lompatan signifikan dalam efisiensi dan keberlanjutan. Memahami mekanisme kerjanya membuka pintu untuk merancang reaksi kimia yang lebih ramah lingkungan dan berkelanjutan.
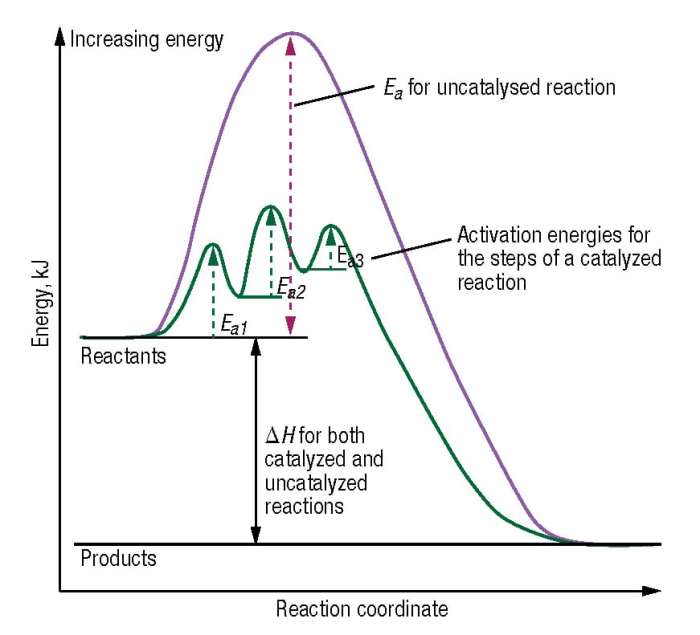
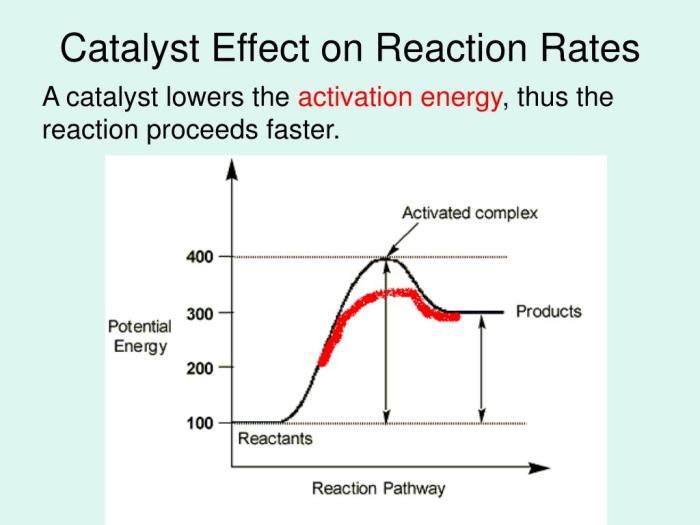
Katalis bekerja dengan menurunkan energi aktivasi, hambatan energi yang harus diatasi agar reaksi dapat berlangsung. Dengan jalan yang lebih rendah ini, lebih banyak molekul reaktan dapat mencapai keadaan transisi dan bereaksi, sehingga laju reaksi meningkat drastis. Jenis katalis beragam, dari yang homogen yang bercampur dengan reaktan hingga heterogen yang membentuk fase terpisah. Pengaruh faktor-faktor seperti suhu, tekanan, dan luas permukaan katalis juga sangat signifikan terhadap efektivitasnya. Pengembangan katalis baru yang lebih efisien dan ramah lingkungan menjadi fokus riset terkini, mengarah pada inovasi berkelanjutan di berbagai sektor industri dan kehidupan sehari-hari.
Pengertian Katalis dan Reaksi Kimia
Katalis, komponen kunci dalam banyak proses kimia, berperan krusial dalam mempercepat laju reaksi tanpa ikut bereaksi secara permanen. Kehadirannya menentukan efisiensi berbagai proses industri, mulai dari produksi bahan bakar hingga pembuatan obat-obatan. Memahami perannya berarti memahami inti dari reaksi kimia itu sendiri. Mari kita telusuri lebih dalam tentang peran katalis ini.
Definisi Katalis dan Contohnya
Katalis adalah zat yang meningkatkan laju reaksi kimia tanpa mengalami perubahan kimiawi permanen. Artinya, katalis dapat digunakan berulang kali dalam reaksi yang sama. Contoh sederhana dalam kehidupan sehari-hari adalah enzim dalam tubuh kita. Enzim-enzim ini bertindak sebagai katalis biologis, mempercepat reaksi metabolisme yang vital bagi kelangsungan hidup. Contoh lainnya adalah platinum dalam konverter katalitik mobil, yang membantu mengubah gas buang yang berbahaya menjadi senyawa yang kurang berbahaya. Penggunaan katalis sangat luas, mulai dari industri makanan hingga teknologi canggih.
Penerapan Katalis dalam Industri dan Kehidupan Sehari-hari
Katalis, senyawa ajaib yang mampu mempercepat reaksi kimia tanpa ikut bereaksi secara permanen, memiliki peran krusial dalam berbagai sektor, dari industri berskala besar hingga aktivitas sehari-hari yang mungkin tak disadari. Penggunaan katalis bukan hanya meningkatkan efisiensi produksi, tetapi juga mengurangi biaya dan dampak lingkungan. Peran katalis yang begitu signifikan ini menunjukkan betapa pentingnya pemahaman mendalam tentang fungsinya.
Katalis, ibarat kunci yang membuka jalan reaksi kimia lebih cepat dan efisien. Ia menurunkan energi aktivasi, sehingga reaksi berlangsung lebih mudah. Analogi ini relevan dengan kehidupan bermasyarakat; keberagaman, layaknya beragam reaktan, membutuhkan “katalis” berupa harmoni untuk bereaksi secara positif. Memahami pentingnya harmoni dalam keberagaman, sebagaimana dijelaskan dalam artikel mengapa dalam masyarakat yang memiliki keberagaman diperlukan harmoni , crucial untuk menciptakan sinergi.
Tanpa harmoni, reaksi sosial bisa berjalan lambat, bahkan terhambat. Begitu pula dalam reaksi kimia, tanpa katalis yang tepat, reaksi akan berjalan lamban atau bahkan tidak terjadi sama sekali. Jadi, peran katalis, baik dalam reaksi kimia maupun dalam dinamika sosial, sangatlah vital.
Contoh Penerapan Katalis dalam Industri
Berbagai industri memanfaatkan katalis untuk mengoptimalkan proses produksi. Kehadiran katalis memungkinkan reaksi berlangsung lebih cepat dan efisien, menghasilkan produk dengan kualitas yang lebih baik dan biaya yang lebih rendah. Berikut beberapa contohnya:
- Industri Petrokimia: Katalis zeolit digunakan dalam proses cracking untuk memecah molekul hidrokarbon berantai panjang menjadi molekul yang lebih pendek, menghasilkan bensin dan bahan bakar lainnya. Sementara itu, katalis platinum dan logam mulia lainnya berperan dalam proses reforming untuk meningkatkan kualitas bensin, meningkatkan nilai oktan.
- Industri Kimia: Dalam produksi amonia (proses Haber-Bosch), katalis besi digunakan untuk mengoptimalkan sintesis amonia dari nitrogen dan hidrogen. Reaksi ini sangat penting untuk produksi pupuk. Proses ini, meskipun sudah lama dikenal, terus dioptimalkan dengan pengembangan katalis yang lebih efisien dan ramah lingkungan.
- Industri Farmasi: Banyak reaksi sintesis obat memerlukan katalis untuk menghasilkan produk dengan kemurnian tinggi dan rendemen yang optimal. Katalis yang digunakan beragam, tergantung pada jenis reaksi dan senyawa yang terlibat. Keberhasilan sintesis obat baru seringkali bergantung pada penemuan katalis yang tepat.
Katalis dalam Konverter Katalitik Kendaraan Bermotor, Bagaimana peranan katalis dalam mempercepat laju reaksi
Konverter katalitik merupakan contoh nyata penerapan katalis dalam kehidupan modern. Komponen penting dalam sistem pembuangan kendaraan bermotor ini menggunakan katalis logam mulia seperti platinum, palladium, dan rhodium untuk mengubah gas buang yang berbahaya, seperti karbon monoksida (CO), hidrokarbon (HC), dan nitrogen oksida (NOx), menjadi zat yang kurang berbahaya, yaitu karbon dioksida (CO2), air (H2O), dan nitrogen (N2). Efisiensi konverter katalitik sangat berpengaruh pada kualitas udara.
Katalis, layaknya kunci yang membuka pintu reaksi kimia, mempercepat proses tanpa ikut bereaksi secara permanen. Analogi ini mengingatkan kita pada pentingnya peran pendidikan dalam membentuk karakter individu; bagaimana pendidikan dapat menjadi katalis perubahan, sebagaimana diulas dalam artikel pertanyaan tentang pendidikan karakter , untuk mencapai potensi optimal. Sama halnya dengan katalis yang menurunkan energi aktivasi, pendidikan karakter yang efektif dapat mempermudah jalan menuju pembentukan pribadi yang unggul.
Intinya, katalis dan pendidikan karakter sama-sama berperan sebagai akselerator menuju hasil yang lebih baik dan efisien.
Skema Sederhana Proses Cracking dalam Industri Petrokimia
Berikut ilustrasi sederhana proses cracking menggunakan katalis zeolit:
| Tahap | Deskripsi |
|---|---|
| 1. Umpan | Hidrokarbon berantai panjang (misalnya, kerosen) dimasukkan ke dalam reaktor. |
| 2. Kontak dengan Katalis | Hidrokarbon berkontak dengan katalis zeolit pada suhu dan tekanan tinggi. |
| 3. Reaksi Cracking | Katalis zeolit mempercepat pemecahan molekul hidrokarbon berantai panjang menjadi molekul yang lebih pendek (bensin, gas). |
| 4. Pemisahan Produk | Produk reaksi dipisahkan berdasarkan titik didihnya. |
| 5. Produk | Bensin, gas, dan produk lainnya diperoleh. |
Penerapan Katalis dalam Kehidupan Sehari-hari
Katalis tidak hanya berperan dalam industri besar, tetapi juga hadir dalam kehidupan sehari-hari, meskipun kita mungkin tidak menyadarinya. Kehadirannya seringkali tersembunyi dalam berbagai produk dan proses.
Katalis, ibarat kunci sukses reaksi kimia, mampu mempercepat laju reaksi tanpa ikut bereaksi. Prosesnya mirip dengan bagaimana panitia sekolah mencoba mempercepat komunikasi penting dengan orang tua siswa, dengan mengirimkan surat resmi; baca selengkapnya di sini mengapa panitia merasa perlu menulis surat kepada wali murid untuk memahami urgensi komunikasi tersebut. Kembali ke katalis, efektivitasnya bergantung pada sifat dan konsentrasi, sebagaimana efektivitas surat bergantung pada kejelasan informasi dan jangkauan distribusi.
Singkatnya, katalis dan surat, keduanya alat percepatan yang efektif dalam konteks masing-masing.
- Enzim dalam tubuh: Enzim merupakan katalis biologis yang mempercepat reaksi biokimia dalam tubuh kita. Tanpa enzim, banyak proses metabolisme tidak akan berlangsung secepat dan seefisien yang seharusnya.
- Katalis dalam deterjen: Beberapa deterjen mengandung enzim sebagai katalis untuk membantu menghilangkan noda pada pakaian.
- Katalis dalam sel bahan bakar: Sel bahan bakar, yang digunakan dalam beberapa kendaraan, menggunakan katalis untuk mempercepat reaksi elektrokimia yang menghasilkan listrik.
Faktor-faktor yang Mempengaruhi Aktivitas Katalis: Bagaimana Peranan Katalis Dalam Mempercepat Laju Reaksi
Katalis, meskipun berperan krusial dalam mempercepat reaksi kimia, performanya tak selamanya konstan. Berbagai faktor lingkungan dan karakteristik katalis itu sendiri dapat secara signifikan memengaruhi efektivitasnya. Memahami faktor-faktor ini penting, tak hanya untuk optimasi proses industri, tetapi juga untuk pengembangan katalis yang lebih efisien dan berkelanjutan. Mari kita telusuri lebih dalam beberapa faktor kunci yang menentukan kinerja katalis.
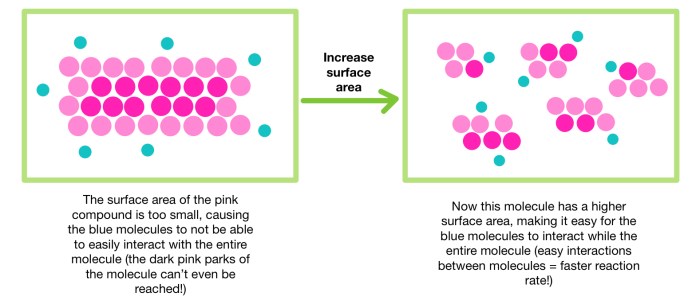
Luas Permukaan Katalis
Luas permukaan katalis berbanding lurus dengan aktivitasnya. Semakin besar luas permukaan, semakin banyak molekul reaktan yang dapat berinteraksi dengan situs aktif katalis dalam waktu yang sama. Bayangkan sebuah butiran katalis berbentuk kubus: jika kita membagi kubus tersebut menjadi kubus-kubus yang lebih kecil, luas permukaan totalnya akan meningkat drastis. Hal ini analog dengan penggunaan katalis dalam bentuk serbuk atau nanopartikel yang memiliki luas permukaan jauh lebih besar dibandingkan katalis dalam bentuk bongkahan besar, sehingga reaksi berlangsung lebih cepat. Peningkatan luas permukaan ini secara langsung meningkatkan frekuensi tumbukan efektif antara reaktan dan situs aktif, yang pada akhirnya mempercepat laju reaksi.
Pengembangan Katalis Baru
Perkembangan katalis baru menjadi kunci dalam berbagai sektor industri, mulai dari energi terbarukan hingga produksi bahan kimia yang lebih ramah lingkungan. Tantangannya tidak hanya sebatas meningkatkan efisiensi, tetapi juga mendesain katalis yang berkelanjutan dan meminimalisir dampak negatif terhadap lingkungan. Inovasi dalam material dan metode sintesis menjadi faktor penentu dalam mencapai tujuan tersebut. Berikut beberapa aspek penting dalam pengembangan katalis baru yang lebih baik.
Tantangan Pengembangan Katalis yang Efisien dan Ramah Lingkungan
Pengembangan katalis baru menghadapi berbagai tantangan kompleks. Salah satu yang utama adalah mencapai selektivitas tinggi, di mana katalis hanya mengkatalisis reaksi yang diinginkan tanpa menghasilkan produk sampingan yang tidak diinginkan. Selain itu, stabilitas katalis dalam kondisi reaksi yang keras, seperti suhu dan tekanan tinggi, juga menjadi faktor krusial. Tantangan lain yang tak kalah penting adalah memperoleh katalis dengan aktivitas tinggi, yang mampu mempercepat reaksi secara signifikan dengan jumlah yang sedikit. Terakhir, aspek ekonomi dan keberlanjutan menjadi perhatian utama, di mana katalis harus terjangkau, mudah disintesis, dan ramah lingkungan, meminimalisir limbah berbahaya.
Peran Nanoteknologi dalam Pengembangan Katalis
Nanoteknologi menawarkan peluang besar dalam merancang katalis dengan kinerja yang superior. Dengan mengendalikan ukuran partikel katalis pada skala nano, luas permukaan yang sangat besar dapat dicapai, yang secara langsung meningkatkan aktivitas katalitik. Modifikasi permukaan nanopartikel juga memungkinkan penyesuaian sifat katalis, seperti selektivitas dan stabilitas. Contohnya, penggunaan nanopartikel logam mulia seperti platinum atau palladium dalam katalis otomotif telah terbukti meningkatkan efisiensi konverter katalitik dalam mengurangi emisi gas buang. Penggunaan material berbasis karbon seperti nanotube karbon dan grafen juga menjanjikan peningkatan kinerja katalis.
Contoh Katalis Baru dan Aplikasinya
Berbagai katalis baru telah dikembangkan dengan aplikasi yang beragam. Salah satu contohnya adalah katalis berbasis logam transisi yang digunakan dalam reaksi hidrogenasi, yang penting dalam produksi bahan kimia dan farmasi. Katalis ini seringkali di-doping dengan unsur lain untuk meningkatkan aktivitas dan selektivitasnya. Katalis fotokatalitik berbasis titanium dioksida (TiO2) telah banyak digunakan dalam pengolahan air limbah dan pemurnian udara karena kemampuannya untuk mendegradasi polutan organik menggunakan energi cahaya. Penelitian terbaru juga fokus pada pengembangan katalis untuk reaksi elektrokimia, seperti dalam produksi hidrogen dari air (elektrolisis air) dan baterai bahan bakar.
Metode Sintesis Katalis
Sintesis katalis melibatkan berbagai metode, masing-masing dengan kelebihan dan kekurangannya. Metode sol-gel, misalnya, memungkinkan pembuatan material katalis dengan ukuran partikel dan pori yang terkontrol. Metode presipitasi merupakan metode yang sederhana dan relatif murah, namun kontrol atas ukuran partikel dan morfologi katalis mungkin kurang presisi. Metode templat memungkinkan pembuatan material katalis dengan struktur yang sangat terorganisir. Teknik hidrotermal dan solvotermal digunakan untuk mensintesis material katalis pada suhu dan tekanan tinggi, memungkinkan pembentukan fase kristal tertentu. Pilihan metode sintesis bergantung pada jenis katalis yang diinginkan dan sifat-sifat yang dibutuhkan.
Perkembangan Terkini Riset Katalis
Penelitian terkini dalam bidang katalis terus berkembang pesat. Sebuah studi di jurnal Nature Catalysis (misalnya) menunjukkan potensi katalis tunggal atom dalam meningkatkan efisiensi reaksi tertentu. Studi tersebut menyoroti pentingnya mengoptimalkan struktur dan lingkungan atom tunggal untuk mencapai aktivitas katalitik yang maksimal. Perkembangan ini membuka jalan bagi desain katalis yang lebih efisien dan ramah lingkungan di masa depan. Studi lain yang diterbitkan di jurnal ACS Catalysis (misalnya) meneliti penggunaan kecerdasan buatan (AI) untuk merancang dan mengoptimalkan katalis baru. AI dapat mempercepat proses penemuan katalis dengan memprediksi kinerja katalis berdasarkan struktur dan sifatnya. Hal ini menjanjikan kemajuan yang signifikan dalam pengembangan katalis di masa depan.
Akhir Kata
Kesimpulannya, peranan katalis dalam mempercepat laju reaksi tak terbantahkan. Katalis, ibarat kunci yang membuka pintu menuju reaksi kimia yang lebih cepat dan efisien. Dari industri petrokimia hingga kendaraan bermotor, katalis telah merevolusi berbagai proses produksi. Namun, perjalanan menuju katalis yang lebih ramah lingkungan dan efisien masih terus berlanjut. Riset dan pengembangan terus dilakukan untuk mengatasi tantangan dalam menciptakan katalis yang lebih selektif, tahan lama, dan berdampak minimal terhadap lingkungan. Memahami bagaimana katalis bekerja adalah kunci untuk menciptakan inovasi yang berkelanjutan dan meningkatkan kualitas hidup manusia.
 TendikPedia Informasi Mengenai Pendidikan yang Akurat dan Terpercaya
TendikPedia Informasi Mengenai Pendidikan yang Akurat dan Terpercaya



