PCl3 polar atau nonpolar? Pertanyaan ini mengantar kita pada dunia kimia yang menarik, di mana struktur molekul menentukan sifat-sifatnya. Memahami polaritas PCl3, senyawa fosfor triklorida, bukan hanya sekadar mempelajari teori, tetapi juga kunci untuk mengungkap perilakunya dalam reaksi kimia dan aplikasinya di berbagai bidang. Dari geometri molekul hingga perhitungan momen dipol, perjalanan kita akan mengupas tuntas sifat polaritas PCl3 dan membandingkannya dengan senyawa sejenis. Siapkan diri untuk menyelami detail molekul ini, karena pemahaman mendalam akan mengungkap rahasia di balik sifat-sifatnya yang unik.
Fosfor triklorida (PCl3) merupakan senyawa kimia yang menarik perhatian karena sifat polaritasnya. Analisis mendalam terhadap struktur molekulnya, khususnya geometri dan distribusi elektron, menjadi kunci untuk menentukan apakah PCl3 bersifat polar atau nonpolar. Perbedaan elektronegativitas antara atom fosfor (P) dan klor (Cl) memainkan peran krusial dalam menentukan momen dipol ikatan dan momen dipol total molekul. Dengan memahami konsep-konsep ini, kita dapat menjelaskan perilaku PCl3 dalam berbagai reaksi dan aplikasinya.
Struktur Molekul PCl3

Fosfor triklorida (PCl3), sebuah senyawa kimia yang menarik, memiliki sifat-sifat yang dipengaruhi langsung oleh struktur molekulnya. Pemahaman mendalam tentang geometri dan distribusi elektron dalam molekul ini krusial untuk menjelaskan polaritasnya. Analisis struktur PCl3 akan mengungkap mengapa senyawa ini menunjukkan perilaku polar, bukan nonpolar. Perjalanan kita akan dimulai dengan mengkaji struktur Lewis-nya, kemudian menelusuri geometri molekul dan implikasinya terhadap polaritas.
Struktur Lewis PCl3
Struktur Lewis PCl3 menggambarkan bagaimana atom-atom terikat dan elektron valensi terdistribusi. Fosfor (P), sebagai atom pusat dengan lima elektron valensi, berikatan secara kovalen dengan tiga atom klor (Cl), masing-masing menyumbangkan satu elektron untuk membentuk ikatan tunggal. Sisa dua elektron valensi fosfor membentuk pasangan elektron bebas. Representasi visualnya menunjukkan atom fosfor di tengah, dikelilingi oleh tiga atom klor dan satu pasangan elektron bebas. Susunan ini menjadi kunci untuk memahami geometri molekul selanjutnya.
Elektronegativitas Atom Penyusun
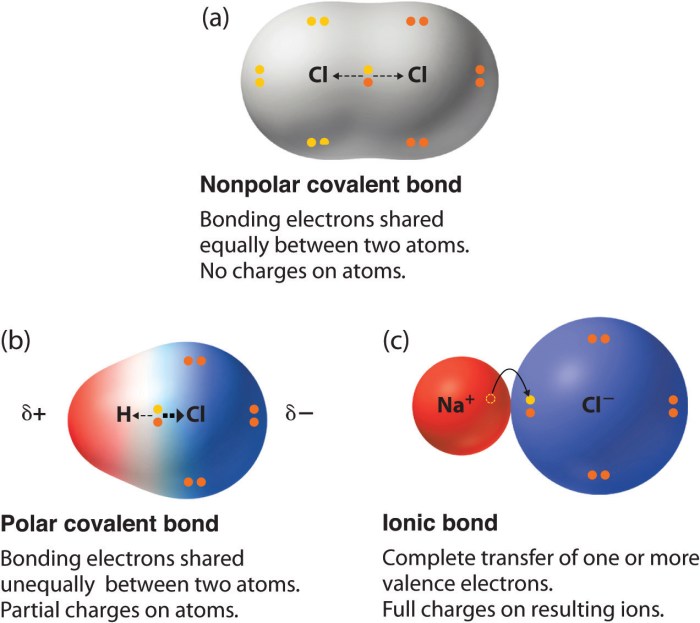
Untuk memahami polaritas molekul PCl3, pemahaman mendalam tentang elektronegativitas atom penyusunnya, fosfor (P) dan klor (Cl), sangat krusial. Perbedaan elektronegativitas ini menentukan sebaran muatan dalam ikatan dan, pada akhirnya, menentukan apakah molekul tersebut bersifat polar atau nonpolar. Analisis ini akan mengungkap bagaimana perbedaan sifat dasar atom-atom tersebut membentuk karakteristik molekul PCl3.
Perbedaan elektronegativitas antara dua atom dalam sebuah ikatan kimia menentukan sifat polar atau nonpolar dari ikatan tersebut. Semakin besar perbedaan elektronegativitas, semakin polar ikatannya. Sebaliknya, jika perbedaannya kecil atau mendekati nol, ikatan cenderung bersifat nonpolar. Hal ini karena atom yang lebih elektronegatif akan menarik elektron ikatan lebih kuat, menciptakan dipol dengan muatan parsial negatif (δ-) pada atom yang lebih elektronegatif dan muatan parsial positif (δ+) pada atom yang kurang elektronegatif.
PCl 3, dengan geometri trigonal piramida dan perbedaan elektronegativitas antara fosfor dan klorin, merupakan molekul polar. Pemahaman konsep kepolaran ini krusial, bahkan dalam konteks pembelajaran daring. Untuk mencari informasi lebih lanjut tentang sumber daya pendidikan daring, silahkan cek nama domain yang digunakan untuk pendidikan adalah , yang mungkin membantu menjelaskan berbagai platform pembelajaran. Kembali ke PCl 3, sifat polarnya memengaruhi sifat fisik dan kimianya, membuatnya berinteraksi berbeda dengan molekul lain dibandingkan dengan senyawa nonpolar.
Perbandingan Elektronegativitas Fosfor dan Klor
Skala Pauling merupakan skala yang umum digunakan untuk mengukur elektronegativitas. Berdasarkan skala ini, elektronegativitas fosfor (P) sekitar 2,19, sedangkan elektronegativitas klor (Cl) sekitar 3,16. Terlihat jelas perbedaan yang cukup signifikan antara kedua nilai tersebut.
| Atom | Elektronegativitas (Skala Pauling) |
|---|---|
| Fosfor (P) | 2,19 |
| Klor (Cl) | 3,16 |
Perbedaan elektronegativitas sebesar 3,16 – 2,19 = 0,97 menunjukkan bahwa ikatan P-Cl bersifat polar. Atom klor, yang lebih elektronegatif, menarik elektron ikatan lebih kuat daripada atom fosfor. Akibatnya, terbentuk dipol dengan muatan parsial negatif (δ-) pada atom klor dan muatan parsial positif (δ+) pada atom fosfor dalam setiap ikatan P-Cl.
Pengaruh Perbedaan Elektronegativitas terhadap Polaritas Ikatan
Besarnya perbedaan elektronegativitas secara langsung memengaruhi momen dipol ikatan. Momen dipol adalah ukuran kekuatan dan arah polaritas suatu ikatan. Ia dihitung dengan mengalikan besarnya muatan parsial dengan jarak antara muatan parsial positif dan negatif. Semakin besar perbedaan elektronegativitas, semakin besar momen dipol ikatan, dan semakin polar ikatan tersebut.
Meskipun setiap ikatan P-Cl dalam PCl3 bersifat polar, geometri molekul juga berperan penting dalam menentukan polaritas keseluruhan molekul. Geometri molekul PCl3 adalah piramida trigonal, dengan atom fosfor berada di pusat dan tiga atom klor berada di sudut-sudut piramida. Meskipun terdapat tiga dipol ikatan P-Cl, arah dipol ini tidak saling meniadakan karena geometri molekulnya yang asimetris. Akibatnya, molekul PCl3 memiliki momen dipol total yang tidak nol, dan karenanya bersifat polar.
Momen Dipol Ikatan P-Cl
Meskipun perhitungan tepat momen dipol memerlukan metode-metode kuantum yang kompleks, dapat disimpulkan bahwa momen dipol ikatan P-Cl memiliki nilai yang cukup signifikan karena perbedaan elektronegativitas yang cukup besar antara fosfor dan klor. Nilai ini berkontribusi pada momen dipol total molekul PCl3, yang membuatnya bersifat polar.
Momen Dipol dan Polaritas Molekul PCl3
Fosfor triklorida (PCl3), sebuah senyawa kimia yang cukup penting dalam berbagai aplikasi industri, memiliki karakteristik polaritas yang menarik untuk dikaji. Pemahaman mendalam tentang momen dipol dan bagaimana hal itu menentukan polaritas molekul sangat krusial, terutama dalam memprediksi sifat-sifat fisik dan kimia senyawa tersebut. Analisis ini akan menguraikan secara detail bagaimana momen dipol ikatan individu berkontribusi pada momen dipol total molekul PCl3, dan bagaimana hal ini menentukan sifat polarnya.
Polaritas molekul, singkatnya, adalah gambaran sebaran muatan listrik dalam molekul. Jika sebaran muatan tidak merata, maka molekul bersifat polar. Sebaliknya, jika sebaran muatan merata, molekul bersifat nonpolar. PCl3, dengan struktur geometri piramida trigonalnya, menunjukkan kasus menarik dari interaksi momen dipol. Perbedaan elektronegativitas antara atom fosfor (P) dan klorin (Cl) menciptakan momen dipol pada setiap ikatan P-Cl.
Momen Dipol Ikatan Individual dalam PCl3
Perbedaan elektronegativitas antara atom fosfor (P) dan klorin (Cl) merupakan kunci untuk memahami momen dipol ikatan individual dalam PCl3. Klorin lebih elektronegatif daripada fosfor, sehingga elektron ikatan lebih tertarik ke arah atom klorin. Hal ini menghasilkan muatan parsial negatif (δ-) pada atom klorin dan muatan parsial positif (δ+) pada atom fosfor untuk setiap ikatan P-Cl. Setiap ikatan P-Cl memiliki momen dipol yang mengarah dari atom fosfor (kutub positif) ke atom klorin (kutub negatif).
Perhitungan Momen Dipol Total PCl3
Momen dipol total molekul PCl3 merupakan resultan vektor dari momen dipol ikatan individual. Karena molekul PCl3 memiliki geometri piramida trigonal, momen dipol ikatan individual tidak saling meniadakan. Mereka berinteraksi dan menghasilkan momen dipol total yang tidak nol. Perhitungan yang tepat membutuhkan pengetahuan tentang besarnya momen dipol ikatan P-Cl dan sudut ikatan. Secara sederhana, dapat divisualisasikan sebagai penjumlahan vektor dari tiga momen dipol ikatan P-Cl yang membentuk resultan yang menunjuk ke arah bawah, menjauhi atom fosfor. Resultan ini menggambarkan momen dipol total molekul yang tidak nol.
PCl 3, dengan geometri trigonal piramida, bersifat polar karena perbedaan elektronegativitas antara fosfor dan klor menghasilkan momen dipol resultan. Memahami konsep kepolaran ini penting, apalagi jika kita membahasnya dalam konteks pembelajaran kimia di berbagai apa yang dimaksud institusi pendidikan , mulai dari sekolah menengah hingga universitas. Institusi pendidikan, dengan beragam program studi, memiliki peran krusial dalam membentuk pemahaman konsep-konsep dasar sains seperti ini.
Kembali ke PCl 3, kepolarannya mempengaruhi sifat fisik dan kimia senyawa ini, menentukan interaksi antarmolekul dan reaktivitasnya.
Hubungan Momen Dipol Total dan Polaritas Molekul
Adanya momen dipol total yang tidak nol dalam PCl3 secara langsung menunjukkan bahwa molekul ini bersifat polar. Ini berarti terdapat distribusi muatan yang tidak merata dalam molekul. Bagian molekul di sekitar atom klorin memiliki muatan parsial negatif yang lebih besar dibandingkan dengan bagian molekul di sekitar atom fosfor. Sifat polar ini berpengaruh signifikan terhadap sifat-sifat fisik dan kimia PCl3, seperti titik didih, kelarutan, dan reaktivitas.
Diagram Vektor Momen Dipol PCl3, Pcl3 polar atau nonpolar
Bayangkan sebuah piramida trigonal dengan atom fosfor di puncak dan tiga atom klorin di dasar. Tiga vektor, masing-masing mewakili momen dipol ikatan P-Cl, mengarah dari atom fosfor ke masing-masing atom klorin. Karena sudut ikatan dalam PCl3 kurang dari 120 derajat, vektor-vektor ini tidak saling meniadakan. Resultan dari ketiga vektor ini adalah momen dipol total, yang mengarah ke bawah, menjauhi atom fosfor dan menuju pusat dari tiga atom klorin. Ilustrasi ini menunjukkan secara visual bagaimana momen dipol ikatan individu berkontribusi pada momen dipol total yang menghasilkan polaritas molekul.
Distribusi Muatan dalam Molekul PCl3
Momen dipol total berhubungan langsung dengan distribusi muatan dalam molekul. Karena PCl3 bersifat polar, distribusi muatannya tidak merata. Atom klorin yang lebih elektronegatif menarik elektron ikatan lebih kuat, menghasilkan kerapatan elektron yang lebih tinggi di sekitar atom klorin. Akibatnya, atom klorin memiliki muatan parsial negatif (δ-), sementara atom fosfor memiliki muatan parsial positif (δ+). Distribusi muatan yang tidak merata ini bertanggung jawab atas sifat-sifat polar PCl3 dan interaksi antarmolekulnya.
Perbandingan Polaritas PCl3 dengan Molekul Lain
Memahami polaritas molekul merupakan kunci untuk mengungkap sifat-sifat fisik dan kimia suatu zat. Fosfor triklorida (PCl3), sebagai molekul dengan geometri piramida trigonal, memiliki polaritas yang signifikan. Namun, bagaimana polaritasnya dibandingkan dengan molekul serupa seperti fosfor pentaklorida (PCl5) dan fosfor trifluorida (PF3)? Perbandingan ini akan memberikan gambaran yang lebih komprehensif tentang bagaimana struktur molekul memengaruhi sifat-sifatnya.
PCl 3, dengan geometri trigonal piramida, memiliki momen dipol yang signifikan, membuatnya bersifat polar. Ini berbeda dengan molekul simetris yang cenderung nonpolar. Memahami konsep kepolaran ini penting, bahkan bagi para pendidik. Sebab, konsep ini diajarkan di sekolah, mengingatkan kita bahwa profesi guru, sebagaimana dijelaskan dalam artikel guru merupakan pekerjaan di bidang pendidikan, membutuhkan pemahaman mendalam atas berbagai ilmu, termasuk kimia.
Kembali ke PCl 3, kepolarannya mempengaruhi sifat fisik dan kimianya, menunjukkan betapa pentingnya memahami struktur molekul untuk memprediksi sifat-sifatnya.
Perbedaan struktur geometri dan elektronegativitas atom penyusunnya menjadi faktor utama perbedaan polaritas antar molekul ini. Analisis mendalam akan menunjukkan bagaimana perbedaan tersebut berdampak pada titik didih, kelarutan, dan reaktivitas senyawa-senyawa tersebut.
Struktur dan Polaritas PCl3, PCl5, dan PF3
PCl3 memiliki geometri piramida trigonal, dengan pasangan elektron bebas pada atom fosfor. Kehadiran pasangan elektron bebas ini menyebabkan distribusi muatan tidak merata, menghasilkan molekul polar. Sebaliknya, PCl5 memiliki geometri bipiramida trigonal, distribusi muatannya lebih simetris sehingga cenderung nonpolar, meskipun perbedaan elektronegativitas antara fosfor dan klor masih ada. Sementara PF3, mirip dengan PCl3 dalam hal geometri piramida trigonal, namun memiliki polaritas yang lebih tinggi karena fluor lebih elektronegatif daripada klor.
Tabel Perbandingan Polaritas
| Molekul | Geometri Molekul | Polaritas | Alasan |
|---|---|---|---|
| PCl3 | Piramida Trigonal | Polar | Pasangan elektron bebas pada P dan perbedaan elektronegativitas P-Cl |
| PCl5 | Bipiramida Trigonal | Nonpolar (atau sedikit polar) | Distribusi elektron yang relatif simetris |
| PF3 | Piramida Trigonal | Polar (lebih polar daripada PCl3) | Perbedaan elektronegativitas P-F yang lebih besar |
Pengaruh Perbedaan Polaritas terhadap Sifat Fisik dan Kimia
Perbedaan polaritas ini berdampak signifikan pada sifat fisik dan kimia ketiganya. Misalnya, titik didih PCl3 lebih tinggi daripada PCl5 karena adanya gaya antarmolekul dipol-dipol pada PCl3 yang lebih kuat dibandingkan gaya London pada PCl5. Kelarutan dalam pelarut polar juga akan berbeda, dengan PCl3 lebih mudah larut dalam pelarut polar daripada PCl5. Reaktivitasnya pun dipengaruhi oleh polaritas; PCl3, sebagai molekul polar, cenderung lebih reaktif dalam reaksi tertentu dibandingkan PCl5 yang relatif kurang reaktif.
Perbedaan polaritas antar molekul ini memiliki implikasi penting dalam berbagai aplikasi, mulai dari sintesis senyawa organik hingga industri elektronik. Memahami detail interaksi antarmolekul menjadi kunci dalam merancang dan mengoptimalkan proses kimia. Sebagai contoh, sifat polar PCl3 membuatnya menjadi reagen penting dalam sintesis berbagai senyawa organofosfor.
Aplikasi dan Implikasi Polaritas PCl3: Pcl3 Polar Atau Nonpolar
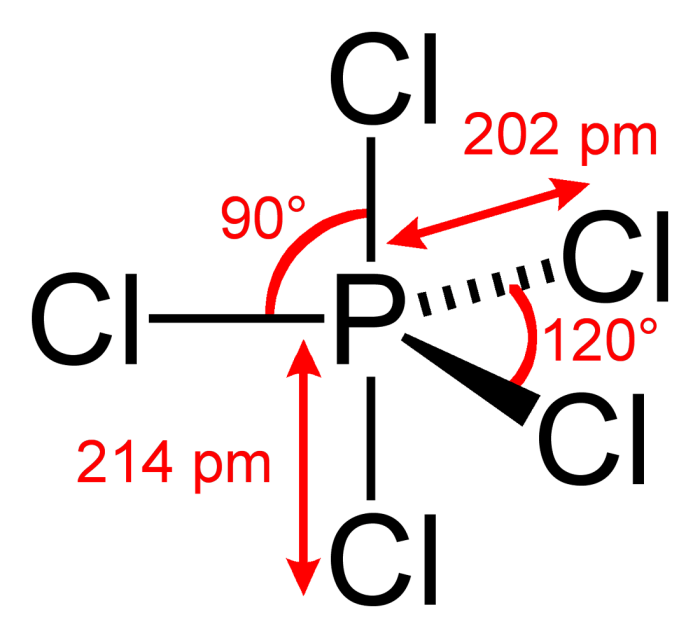
Fosfor triklorida (PCl3), sebuah molekul piramida trigonal dengan momen dipol yang signifikan, memiliki beragam aplikasi yang erat kaitannya dengan sifat polarnya. Polaritas ini mempengaruhi interaksi molekul PCl3 dengan berbagai zat, menentukan kelarutannya, dan mempengaruhi reaktivitasnya dalam berbagai reaksi kimia. Pemahaman mendalam tentang bagaimana polaritas ini berperan penting untuk mengoptimalkan penggunaannya dalam berbagai industri.
Aplikasi PCl3 yang Dipengaruhi Polaritasnya
Sifat polar PCl3 membuatnya berperan penting dalam berbagai proses industri. Kemampuannya untuk berinteraksi dengan molekul polar lainnya menjadi kunci keberhasilannya dalam aplikasi-aplikasi spesifik. Berikut beberapa contohnya:
- Sebagai perantara dalam sintesis berbagai senyawa organofosfor, dimana polaritasnya membantu dalam pembentukan ikatan dengan molekul organik polar.
- Digunakan sebagai agen klorinasi dalam produksi pestisida dan beberapa jenis bahan kimia industri lainnya, dengan polaritas yang memfasilitasi reaksi dengan senyawa organik.
- Berperan dalam pembuatan ester fosfat, yang banyak digunakan dalam industri makanan dan farmasi, dimana polaritasnya mempengaruhi interaksi dan reaksi dengan molekul lain selama proses sintesis.
Pengaruh Polaritas PCl3 terhadap Kelarutannya
Seperti senyawa polar pada umumnya, PCl3 lebih mudah larut dalam pelarut polar daripada pelarut nonpolar. Hal ini dikarenakan adanya gaya tarik-menarik dipol-dipol antara molekul PCl3 dan molekul pelarut polar, seperti air atau aseton. Sebaliknya, kelarutannya dalam pelarut nonpolar seperti heksana akan jauh lebih rendah.
Tabel Aplikasi PCl3 dan Kaitannya dengan Polaritas Molekul
| Aplikasi | Kaitan dengan Polaritas |
|---|---|
| Sintesis Organofosfat | Interaksi dipol-dipol dengan reaktan polar memfasilitasi reaksi |
| Agen Klorinasi | Interaksi polar meningkatkan reaktivitas dengan senyawa organik |
| Pembuatan Ester Fosfat | Kelarutan dalam pelarut polar memudahkan proses sintesis |
Pengaruh Polaritas PCl3 terhadap Reaktivitasnya
Reaktivitas PCl3 sangat dipengaruhi oleh polaritasnya. Momen dipol yang signifikan menyebabkan atom fosfor (P) memiliki muatan parsial positif (δ+), sementara atom klorin (Cl) memiliki muatan parsial negatif (δ−). Distribusi muatan ini membuat PCl3 lebih rentan terhadap serangan nukleofilik pada atom fosfor, dan lebih mudah bereaksi dengan senyawa-senyawa yang memiliki gugus elektron kaya.
Interaksi Antarmolekul PCl3
Interaksi antarmolekul PCl3 didominasi oleh gaya dipol-dipol, akibat polaritas molekulnya. Gaya ini lebih kuat dibandingkan gaya London (dispersi), yang umumnya ditemukan pada molekul nonpolar. Interaksi dipol-dipol ini mempengaruhi sifat fisik PCl3, seperti titik didih yang relatif lebih tinggi dibandingkan dengan senyawa nonpolar dengan berat molekul yang sebanding.
Ringkasan Akhir
Kesimpulannya, PCl3 terbukti bersifat polar. Hal ini disebabkan oleh geometri molekulnya yang piramida trigonal dan perbedaan elektronegativitas antara atom fosfor dan klor. Perbedaan ini menghasilkan momen dipol ikatan yang tidak saling meniadakan, sehingga menghasilkan momen dipol total yang signifikan. Pemahaman tentang polaritas PCl3 ini sangat penting dalam berbagai aplikasi, mulai dari sintesis senyawa kimia hingga pemahaman tentang sifat-sifat fisik dan kimianya. Lebih jauh lagi, perbandingan dengan senyawa sejenis seperti PCl5 dan PF3 memperkaya pemahaman kita tentang bagaimana struktur molekul mempengaruhi sifat polaritas dan implikasinya.
 TendikPedia Informasi Mengenai Pendidikan yang Akurat dan Terpercaya
TendikPedia Informasi Mengenai Pendidikan yang Akurat dan Terpercaya